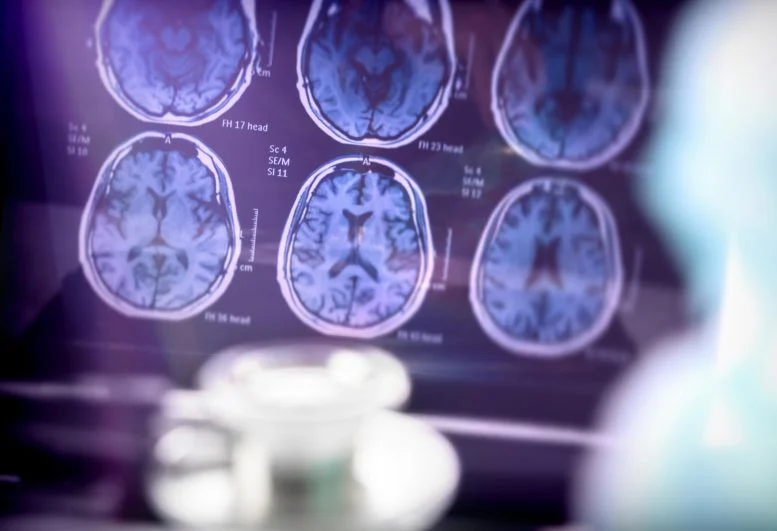
تتحكم الإيقاعات اليومية في إزالة بروتين رئيسي مرتبط بمرض الزهايمر.
Credit: Rensselaer Polytechnic Institute
تتذبذب قدرة الجهاز المناعي على تدمير البروتين المرتبط بمرض الزهايمر مع الإيقاع اليومي اليومي.
وفقًا لبحث نُشر مؤخرًا في مجلة PLOS Genetics، فإن قدرة الدماغ على التخلص من بروتين مرتبط ارتباطًا وثيقًا بمرض
الزهايمر مرتبطة بدورتنا اليومية. ويؤكد البحث على أهمية عادات النوم الصحية في منع بروتين أميلويد بيتا 42 (AB42) من
تكوين كتل في الدماغ، ويفتح الطريق أمام علاجات محتملة لمرض الزهايمر.
قالت جينيفر هيرلي، الخبيرة في الإيقاعات اليومية، والأستاذة المساعدة في العلوم البيولوجية في معهد رينسيلير بوليتكنيك:
" يلعب التنظيم اليومي للخلايا المناعية دورًا في العلاقة المعقدة بين الساعة اليومية ومرض الزهايمر". "يخبرنا هذا أن نمط
النوم الصحي قد يكون مهمًا لتخفيف بعض أعراض مرض الزهايمر، وقد يتم نقل هذا التأثير المفيد من خلال نوع من الخلايا
المناعية يسمى الخلايا البلعمية / الخلايا الدبقية الصغيرة".
أبحاث تركز على الخلايا المناعية وتصفية AB42
أجري البحث في مركز رينسيلير للتكنولوجيا الحيوية والدراسات متعددة التخصصات، والذي يركز على الأمراض العصبية
التنكسية. عمل الدكتور هيرلي مع أساتذة رينسيلير روبرت لينهاردت، خبير الجليكانات ومخترع الهيبارين الاصطناعي،
وتشونيو وانج، الذي قام بحثه الجاري بتفصيل العديد من الآليات في إنتاج وانتشار البروتينات المتورطة في مرض الزهايمر.
"يكشف هذا الاكتشاف عن آلية جديدة ومسار لعلاج الأمراض العصبية التنكسية مثل الزهايمر من خلال نهج متعدد
التخصصات، وهو رمز لقوة مركز أبحاث واكتشافات الخلايا العصبية في مجال البحث والاكتشاف ويوفر زاوية جديدة لصحة
الإنسان ورفاهيته"، كما قال ديباك فاشيشث، مدير مركز أبحاث واكتشافات الخلايا العصبية.
يتكون النظام اليومي من مجموعة أساسية من بروتينات الساعة التي تتوقع دورة الليل والنهار من خلال التسبب في تذبذبات
يومية في مستويات الإنزيمات والهرمونات، مما يؤثر في النهاية على المعايير الفسيولوجية مثل درجة حرارة الجسم
والاستجابة المناعية. يرتبط تعطيل النظام اليومي بشكل متزايد بأمراض مثل مرض السكري والسرطان ومرض الزهايمر.
التحكم اليومي في الخلايا المناعية
تعتبر اللويحات، وهي كتل خارج الخلية من بروتين AB42 في الدماغ، من العلامات الواضحة لمرض الزهايمر. الخلايا
البلعمية (والتي يشار إليها باسم الخلايا الدبقية الصغيرة عندما تكون موجودة في الدماغ)، وهي خلايا مناعية تبحث عن المواد
غير المرغوب فيها وتدمرها، تزيل AB42 من الدماغ عن طريق تناولها في عملية تسمى البلعمة. في بحث سابق، قام الدكتور
هيرلي وزملاؤه في الكلية الملكية للجراحين في أيرلندا بالتحقيق في التحكم اليومي في الخلايا البلعمية، وجمعوا مجموعة
بيانات شاملة جعلت من الممكن معرفة أي الحمض النووي الريبي والبروتينات في الخلايا البلعمية تتذبذب بإيقاع يومي. لاحظ
الباحثون تذبذبات في الإنزيمات التي تساعد في صنع بروتينين على سطح الخلايا البلعمية - بروتيوجليكان كبريتات الهيباران
وبروتيوجليكان كبريتات الكوندرويتين - وكلاهما معروف بلعبه دورًا في تنظيم إزالة AB42.
هل يمكن أن تكون هذه البروتيوجليكان على سطح الخلايا بمثابة رابط بين النظام اليومي ومرض الزهايمر؟ وفي سلسلة من
التجارب الأنيقة لاختبار هذه الفرضية، أثبت الفريق أن كمية AB42 التي تبتلعها الخلايا البلعمية السليمة تتذبذب مع إيقاع
الساعة البيولوجية اليومي. ولم يحدث هذا النمط في الخلايا البلعمية التي لا تحتوي على ساعة بيولوجية. كما قاموا بقياس
التذبذبات اليومية في مستويات بروتيوجليكان كبريتات الهيباران وبروتيوجليكان كبريتات الكوندرويتين المنتجة على سطح
الخلايا البلعمية ذات الدورات البيولوجية الصحية. وقد حدث ذروة تصفية AB42 عندما كان إنتاج بروتيوجليكان الخلايا
السطحية في أدنى مستوياته، وأدى إزالة هذه البروتيوجليكان إلى زيادة الابتلاع، مما يشير إلى أن البروتيوجليكان تمنع تصفية
AB42.
قال الدكتور هيرلي: "من الواضح أن كل هذا يتم توقيته بواسطة الساعة البيولوجية. عندما يكون هناك الكثير من بروتيوجليكان
سطح الخلية، فإن الخلايا البلعمية لا تبتلع AB42. "نحن لسنا متأكدين من سبب حدوث ذلك، ولكن هناك علاقة بالتأكيد."
إمكانات علاجات الزهايمر
يمكن استخدام هذه العلاقة لتطوير علاجات من شأنها تشجيع إزالة AB42 بشكل أكبر، ربما من خلال تعزيز سعة التذبذبات
اليومية، والتي تميل إلى التضاؤل مع تقدمنا في السن.
"من الناحية النظرية، إذا تمكنا من تعزيز هذا الإيقاع، فربما نتمكن من زيادة إزالة AB42 ومنع تلف الدماغ،" قال الدكتور
هيرلي.
المصدر: